Axit là một chất hóa học có tính ăn mòn cực cao và có thể gây nguy hiểm đến tính mạng người sử dụng. Thậm chí, người sử dụng có thể tử vong nếu tiếp xúc với một lượng lớn axit đặc mà không có biện pháp cứu chữa kịp thời. Trong bài viết này chúng ta sẽ cùng tìm hiểu về axit, cũng như những điều cần biết trước khi sử dụng axit để đảm bảo an toàn khi sử dụng.
Axit là gì?
Định nghĩa axit
Axit là một hợp chất hóa học mà trong thành phần phân tử của các chất đó có chứa một hay nhiều nguyên tử hidro liên kết với gốc axit (ví dụ -Cl, =SO4, -NO3). Khi hòa tan vào nước, axit sẽ tạo thành một hỗn hợp có độ pH nhỏ hơn 7.
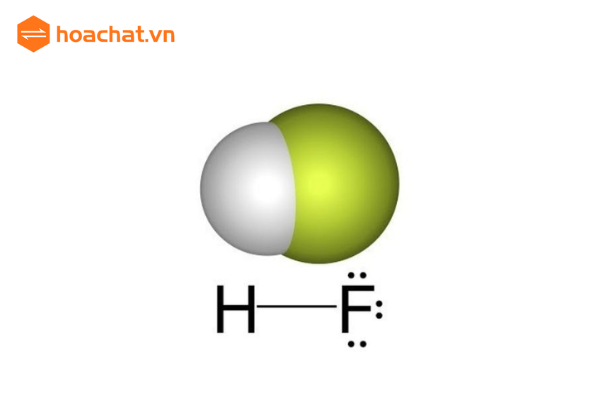
Công thức cấu tạo của axit flohydric
Công thức của axit
Axit có công thức dưới dạng tổng quát như sau: HxA
Trong đó: x là chỉ số nguyên tử của H, và A là gốc của axit, ví dụ:
- Axit cohidric: HCl
- Axit cacbonic: H2CO3
- Axit photphoric: H3PO4
Để hiểu rõ hơn về axit, bạn có thể tham khảo bài viết: Axit là gì? Những kiến thức liên quan đến aixt cần nắm vững
Phân loại
Axit có rất nhiều loại, với các thành phần và công thức hóa học khác nhau kết hợp hình thành.
Dựa vào tính chất hóa học, chúng ta có thể chia axit thành các nhóm bao gồm:
Axit mạnh: Hòa tan loại axit này với các dung dịch khác sẽ tạo ra một dung dịch có độ pH rất thấp và cách xa mức 7. Tính axit càng mạnh, độ ăn mòn càng cao, người dùng càng phải thận trọng khi sử dụng để tránh gây nguy hiểm tới tính mạng (HCL, HNO3, H2SO4…)
Axit yếu: Các loại axit này khi hòa tan vào nước sẽ tạo ra dung dịch có độ pH gần 7, tính axit thấp, ăn mòn yếu. Tuy nhiên, bản chất của axit là ăn mòn, vì vậy người dùng luôn phải đề phòng và đảm bảo các quy tắc khi sử dụng. (H2S. H2CO3…)
Dựa vào nguyên tử Oxi, ta có thể chia axit thành 2 loại, đó là: axit không có oxi (ví dụ như HCl, H2S, HBr, HI, HF…) và axit có oxi (H2SO4, HNO3, H3PO4, H2CO3…).
Ngoài ra, chúng ta còn có thể phân chia axit theo như các dạng như: Axit vô cơ và hữu cơ (như HCL, H2SO4, CH3COOH), các kim loại ở dạng hidrat hóa (như Al(H2O)3 3+, Cu(H20)2 2+…) và các ion (như H+, H3O+, NH4+…).
Tính chất của axit
Tính chất vật lý
Dựa vào cảm giác và hiện tượng vật lý khi axit tác động tới môi trường xung quanh, chúng ta có 3 tính chất vật lý chủ yếu của axit, đó là:
Axit có vị chua nhẹ khi hòa tan vào nước: Đối với các loại axit khác cũng có vị chua tương tự như khi pha chanh với nước, tuy nhiên các loại này không ăn hoặc nếm thử được bởi vì chúng là hóa chất, có thể gây nguy hiểm và ảnh hưởng đến sức khỏe con người.
Axit có tính ăn mòn: tùy vào chủng loại axit, độ đậm đặc của axit và công thức hóa học của axit mà loại hợp chất này sẽ có tính ăn mòn khác nhau. Đối với những axit có độ pH càng lớn, độ ăn mòn sẽ nhẹ hơn. Do vậy, khi không may tiếp xúc với da, chúng ta sẽ cảm thấy mức độ bỏng rát và nóng lên ở vùng da tiếp xúc nhẹ hơn. Đối với những axit có tính ăn mòn mạnh, đậm đặc, thì có thể ăn mòn một số kim loại, và nếu tiếp xúc với da thịt con người, chắc chắn sẽ gây nguy hiểm đến tính mạng.
Axit có tính dẫn điện: axit cũng được kể là một chất điện ly, nên chúng cũng có thể dẫn điện rất tốt. Tiêu biểu cho tính chất vật lý này là ứng dụng của bình ắc quy trong các loại xe máy, xe tải, xe hơi hiện nay. Chúng đều sử dụng loại ắc quy với thành phần chính là dung dịch axit chứa trong bình đựng và có 2 điện cực cộng và trừ nối ra bên ngoài.
Tính chất hóa học
Dựa vào tính chất hóa học, người ta sẽ phân loại thành các dung dịch axit khác nhau. Ví dụ như phản ứng của axit với kim loại nhanh hay chậm, dung dịch axit có dẫn điện tốt hay không… Sau đây là các tính chất hóa học tiêu biểu của axit trong ngành công nghiệp hóa chất.
Axit làm đổi màu chất chỉ thị màu (quỳ tím): Khi nhúng mẩu giấy quỳ tím có chất hóa học chỉ thị màu vào axit, mẩu giấy sẽ nhanh chóng chuyển sang màu đỏ.
Axit tác dụng với kim loại: axit có thể tác dụng được với một số kim loại đứng trước Hidro trong dãy hoạt động hóa học. Vì vậy, nó không tạo ra các phản ứng hóa học khi cho tiếp xúc với Cu, Ag, Au, Pt. Phản ứng hóa học khi axit tiếp xúc với kim loại, đó là sẽ tạo ra muối và giải phóng khí Hidro.
Axit tác dụng với bazơ: tất cả mọi loại axit đều có thể tác dụng với bazơ, phản ứng xảy ra rất mạnh và được gọi là phản ứng trung hòa.
Axit tác dụng với Oxit Bazơ: tất cả các loại axit đều có thể tác dụng với các chất oxit bazơ.
Axit tác dụng với muối: điều kiện để phản ứng này xảy ra đó là muối tham gia phải là muối tan, axit phải là loại axit mạnh. Sau các phản ứng hóa học này sẽ tạo ra muối không tan. Chất sau khi phản ứng phải tạo ra được ít nhất một kết tủa hoặc phải bay hơi.
Đặc biệt, nếu muối mới được tạo ra sau phản ứng là muối tan, chắc chắn axit được tạo ra sẽ có tính chất của một axit yếu.
Ứng dụng của axit trong đời sống
Axit là một hợp chất hóa học đóng vai trò rất quan trọng trong các ngành công nghiệp cũng như trong đời sống con người hiện nay. Loại hóa chất này có một số ứng dụng tiêu biểu, đó là:
Ứng dụng của axit HCL
Trong ngành công nghiệp luyện kim và ứng dụng trong gia đình, axit có thể loại bỏ gỉ sắt trên bề mặt các vật dụng bằng sắt.
Ứng dụng của axit sunfuric là được sử dụng làm chất điện phân trong các loại ắc quy mà xe hơi, xe tải và xe gắn máy sử dụng ngày nay.
Các loại axit mạnh được sử dụng nhiều trong các ngành công nghiệp khai khoáng, đào khoáng sản, là thành phần của các loại thuốc nổ mạnh để đào hầm và phục vụ cho việc khai thác.
Axit được pha chế trở thành chất phụ gia trong chế biến và bảo quản thực phẩm rất thông dụng trong đời sống hàng ngày.
HNO3 tác dụng với amoniac để tạo ra các loại phân bón như amoni nitrat phục vụ đắc lực cho ngành nông nghiệp.
Trong y học, axit còn được pha chế thành các loại hợp chất hóa học khác nhau để phục vụ cho mục đích điều trị các loại bệnh lý từ thông thường cho đến phức tạp rất hiệu quả.
Những lưu ý khi tiếp xúc, sử dụng axit
Ảnh hưởng xấu khi hít phải axit
Trong trường hợp người sử dụng vô tình hít phải khí của axit, hơi đậm đặc của nó sẽ đi vào trong khí quản và gây nên các kích thích rất mạnh trong đường hô hấp, biểu hiện thường là ho, khó thở, không thể hô hấp bình thường, và nguy hiểm hơn có thể dẫn đến phù phổi, sau đó nhanh chóng tử vong. Do vậy, chúng ta cần phải tuân thủ các quy tắc an toàn khi sử dụng hóa chất này.
Các cách xử lý khi cơ thể tiếp xúc với axit
Đôi khi trong quá trình sử dụng axit, chúng ta đã bất cẩn dẫn đến các tiếp xúc ngoài mong muốn với axit. Vì vậy, khi xảy ra sự cố, bạn cần phải làm những điều sau đây để xử lý kịp thời:
- Xịt nước lạnh lên vùng da tiếp xúc với axit trong vòng 20p hoặc hơn để đảm bảo axit đã được rửa trôi.
- Xé bỏ hết quần áo bị dính axit, chú ý hãy thực hiện từ từ để không làm ảnh hưởng và tổn thương đến những vùng da khác.
- Che vùng bị thương tổn bằng băng gạc, thực hiện các bước vô trùng để đảm bảo vết thương an toàn.
- Phải đeo găng tay trong quá trình sơ cứu nạn nhân tiếp xúc với axit để đảm bảo an toàn cho bản thân.
- Liên hệ các cơ sở y tế gần nhất để tiếp tục chữa trị và hồi phục.
Lưu ý khi xử lý cơ thể tiếp xúc trực tiếp với axit
- Không sử dụng khăn lau có sợi khi lau vết thương, các sợi lông và vải khăn sẽ dính vào vết thương gây thêm tình trạng nhiễm trùng.
- Không chườm vết thương với đá lạnh, không làm vỡ các bóng nước do axit gây ra.
- Phòng tránh tối đa với việc cơ thể tiếp xúc với axit trong quá trình sơ cứu.
- Nếu nạn nhân là trẻ em, đặt trẻ vào bồn tắm và xịt nước nhẹ nhàng lên các vết thương để rửa sạch axit.
Những điều cần tránh khi cơ thể tiếp xúc với axit
- Không ngâm vết thương trong nước vì sẽ gây hòa tan axit khiến cho sự ăn mòn lây lan và làm trầm trọng thêm vết thương.
- Không cố gắng cởi bỏ quần áo vì sẽ gây đau đớn càng thêm cho nạn nhân.
- Không sử dụng bơ, dầu, kem đánh răng hoặc những chất khác bôi lên vết thương.
- Không chọc vỡ các bóng nước vết thương vì sẽ gây nhiễm trùng nặng hơn.
Trên đây, chúng tôi đã chia sẻ đến bạn đọc những thông tin quan trọng cần biết trước khi sử dụng axit. Hy vọng bài viết này sẽ cung cấp cho các bạn những thông tin bổ ích, giúp bạn biết cách sử dụng loại hóa chất này một cách an toàn nhất.





